小野薬品は、オープンイノベーションを生命線とし、国内外の先進的なバイオテクノロジー企業やアカデミアと連携しながら、革新的な医薬品の創製に挑戦しています。従来の低分子医薬品や抗体医薬品に加え、核酸医薬や細胞療法などのモダリティ(創薬基盤技術)にも積極的に取り組み、患者さんに新たな治療の選択肢を提供することを目指しています。
低分子・中分子・核酸

バイオロジクス
事例紹介
二重特異性抗体
2014年4月および2018年3月、小野薬品はMerus N.V.社(オランダ・ユトレヒト、以下、「Merus社」) と自己免疫疾患領域における新薬候補の創製を目的とした創薬提携契約を締結しました。 本契約に基づき、当社はMerus社と共同で同社独自のBiclonics®技術を用いた二重特異性抗体の創製に取り組み、ONO-4685およびONO-4915を創出しました。
- ONO-4685は、PD-1とCD3という二つの分子を抗原として認識する二重特異性抗体です。ONO-4685は活性化T細胞の除去、ならびに活性化T細胞の鎮静化を導くことが期待されることから、自己免疫疾患を対象に第Ⅰ相臨床試験を実施中です。また、PD-1を発現するリンパ腫細胞に対して細胞傷害活性を誘導することから、 T細胞リンパ腫を対象に第Ⅰ相臨床試験を実施中です。
- ONO-4915は、PD-1とCD19という二つの分子を抗原として認識する二重特異性抗体です。ONO-4915は、活性化B細胞ならびに活性化T細胞の鎮静化が期待されることから、自己免疫疾患を対象に第Ⅰ相臨床試験を実施中です。
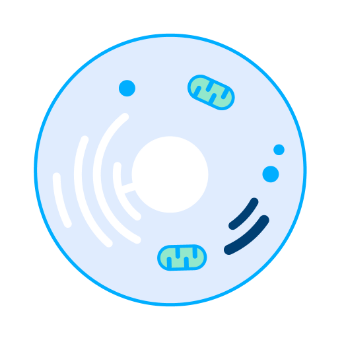
二重特異性抗体とは
自然界に存在する抗体は通常、1つの抗原にしか結合できませんが、二重特異性抗体は、1つの抗体が2つの異なる抗原または同じ抗原の異なる部位に同時に結合できるよう遺伝子組換え技術などを利用して人工的に改変した抗体です。これにより、2つの抗原の機能を同時に阻害したり、特定の細胞を狙った場所に運んだりするなど、従来の抗体医薬では難しかった効果が期待され、がんを中心に様々な疾患の治療薬として研究開発が進められています。
抗体薬物複合体(ADC)
2024年10月、小野薬品はLigaChem Biosciences, Inc.(韓国大田、以下「LCB社」)と固形がん領域における新薬候補LCB97に関するライセンス契約およびLCB社独自の抗体薬物複合体(ADC) 技術ConjuAll™プラットフォームを用いた新規ADC創製に向けた創薬提携契約を締結しました。 LCB97は、複数の固形がんに高発現していることが報告されているL1細胞接着分子(L1CAM)を標的として創製されたファーストインクラスのADCで、これまで治療が困難だったがん患者さんに新たな治療法を届けることを目指したものです。また、 ConjuAll™プラットフォームを用いた新規ADC創製に向けた創薬提携契約では、L1CAMとは異なるがん抗原を標的とした新たなADC の創製を目指しています。
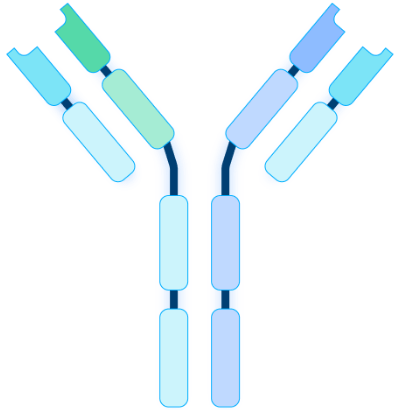
抗体薬物複合体(ADC)とは
抗体薬物複合体(ADC:Antibody-Drug Conjugate)は、特定の細胞を標的とする抗体に高薬理活性化合物を結合させたバイオ医薬品の一種で、近年がん治療法の一つとして注目されています。がん細胞を狙って抗がん剤を直接届けることで従来の化学療法に比べて正常細胞への影響を抑え、副作用を軽減することが期待できます。
細胞療法
2018年9月、小野薬品はFate Therapeutics社(米国・カリフォルニア州、以下「Fate社」)と、iPS細胞由来のキメラ抗原受容体(CAR)-T細胞治療薬の創製を目的とした創薬提携契約を締結しました。この提携は、従来のCAR-T細胞治療薬が抱える固形がん治療における大きな課題―すなわち、腫瘍関連抗原の不均一性や、腫瘍微小環境における免疫抑制、CAR-T細胞の腫瘍への移行効率の低さ―を克服し、これまで治療が困難だったがん患者さんに新たな治療法を届けることを目指したものです。
この提携では、東北大学大学院医学系研究科抗体創薬学分野(加藤 幸成教授)が日本医療研究開発機構(AMED)の先端的バイオ創薬等基盤技術開発事業の成果として取得されたがん選択性を有する新規抗HER2抗体H2CasMab-2と、Fate社の最先端iPS細胞製品プラットフォームを組み合わせて、iPS細胞由来のHER2 CAR-T細胞療法「ONO-8250/FT825」を創製しました。欧米ではFate社と共同で、欧米以外の地域では小野薬品が独占的に開発・商業化を進める体制を確立しており、現在、米国で第Ⅰ相臨床試験を実施しています。
iPS細胞由来CAR-T細胞療法とは
人工多能性幹細胞(iPS細胞)を用いて、がん細胞を認識・攻撃するCAR-T細胞を大量に製造し、患者さんに投与する治療法です。従来のCAR-T細胞療法は、患者さん自身のT細胞を用いるため、個別に細胞を採取し加工する必要がありましたが、Fate社のプラットフォームでは、遺伝子編集を施したiPS細胞から均質なCAR-T細胞を「off-the-shelf(既製品)」として大量生産することが可能です。これにより、患者さんやドナーごとに細胞を採取する必要がなく、安定した品質と供給、コスト面での優位性が期待されます。また、複数の遺伝子編集により、腫瘍への移行性や免疫抑制耐性を高め、固形がんにも有効な治療を目指しています。
(本ページは、2025年12月時点の情報を掲載しています)
